引言:
乳腺癌是全球发病率最高的癌种,在我国也是女性常见的恶性肿瘤,根据 IARC 数据,2020 年全球该癌症新增人数达 226 万人,取代肺癌(220 万)成为全球第一大癌症。近年来,随着我国人口老龄化的加速,工业化、城市化以及生活方式的改变,女性乳腺癌疾病负担日益加重。中国 2020 年乳腺癌发病人数为 41.6 万人,死亡达 11.7 万人,是发病率前三和死亡病例前十的癌种。接下来带大家认识乳腺癌,通过科普可了解自己是否有患癌的风险。
乳腺癌科普:
一:乳腺癌的相关危险因素
1.良性乳腺疾病:如乳腺囊肿和乳腺上皮不典型增生(癌前病变)等
乳腺囊肿增生:乳腺囊肿增生是乳腺组织导管和乳小叶在结构上的退行性病变及进行性结缔组织的生长,其发病原因主要是由于内分泌激素失调。
中医认为:情怀不畅,肝气不得正常疏泻而气滞血淤疾凝,冲任不调者,常有月经紊乱,面部色斑。
现代医学认为:婚育、膳食、人生存的外环境和遗传因素是乳腺发病的主要原因。乳腺囊肿增生与乳腺增生症的区别在于该病增生、不典型增生共存,存在恶变的危险,应视为癌前病变。囊性增生症完全为病理性,组织学改变不可逆。
2.子宫内膜异位症:子宫内膜异位症(endometriosis)是指有活性的内膜细胞种植在子宫内膜以外的位置而形成的一种女性常见妇科疾病。内膜细胞本该生长在子宫腔内,但由于子宫腔通过输卵管与盆腔相通,因此使得内膜细胞可经由输卵管进入盆腔异位生长。目前对此病发病的机制有多种说法,其中被普遍认可的是子宫内膜种植学说。本病多发生于生育年龄的女性,青春期前不发病,绝经后异位病灶可逐渐萎缩退化。
子宫内膜异位症的主要病理变化为异位内膜周期性出血及其周围组织纤维化,形成异位结节,痛经、慢性盆腔痛、月经异常和不孕是其主要症状。病变可以波及所有的盆腔组织和器官,以卵巢、子宫直肠陷凹、宫骶韧带等部位最常见,也可发生于腹腔、胸腔、四肢等处。结果显示,子宫内膜异位症者患乳腺癌的风险为无子宫内膜异位症者的1.04倍(RR:1.04,95% CI:1.00~1.09)。
3.高内源性雌激素水平:无论是绝经前还是绝经后女性,高内源性雌激素水平均会增加乳腺癌的发病风险。对于绝经后女性,激素水平上升与乳腺癌发病风险呈正相关。
注:内源性雌激素水平:由自身体内腺体或细胞分泌的激素称内源性激素。
4.月经生育因素:
①.初潮较早或绝经较晚:初潮年龄较早与乳腺癌发生风险较高有关;绝经年龄每推迟1年,患乳腺癌的相对危险度增加3%。
注:我国女性的平均初潮年龄为13岁
自然绝经年龄为45~55岁之间
②.未经产与初次妊娠的年龄较高:未经产和初次妊娠较晚的女性患乳腺癌的风险增加。一项研究显示,未经产女性患乳腺癌的风险是经产女性的1.32倍.在绝经期或接近绝经期的女性中,与未经产女性相比,首次生产年龄为20岁、25岁和35岁女性乳腺癌的累积发病率(直到70岁)分别降低20%、10%和升高5%。
③.流产:一篇针对有人工流产史中国女性的Meta分析共纳入36篇文献,结果显示,与没有人工流产史的女性相比,有人工流产的女性患乳腺癌的风险增加44%(OR:1.44,95% CI:1.29~1.59),对于人工流产达到2次或2次以上的女性,患乳腺癌风险分别增加76%和89%。
※具备以下任意两项者为乳腺癌高风险人群:
(1)无哺乳史或哺乳时间<4个月;
(2)无活产史(含从未生育、流产、死胎)或初次活产年龄≥30岁;
(3)仅使用“雌激素”的激素替代治疗≥6个月;
(4)流产(含自然流产和人工流产)≥2次。
5.乳腺癌家族史:
Nindrea等对纳入的10项研究进行Meta分析,结果显示,有乳腺癌家族史人群患乳腺癌的风险为正常人群的3.34倍(OR:3.34,95% CI:2.68~4.15);Vishwakarma等对纳入的21 511例乳腺癌患者进行分析,结果显示,有乳腺癌家族史的人群乳腺癌发病风险为健康人群的5.33倍(OR:5.33,95% CI:2.89~9.82)。
※具备以下任意一项者为乳腺癌高风险人群:
(1)一级亲属有乳腺癌或卵巢癌史;
(2)二级亲属50岁前,患乳腺癌2人及以上;
(3)二级亲属50岁前,患卵巢癌2人及以上;
(4)至少1位一级亲属携带已知BRCA1/2基因致病性遗传突变;或自身携带BRCA1/2基因致病性遗传突变。
注1:一级亲属指母亲、女儿以及姐妹。
注2:二级亲属指姑、姨、祖母和外祖母。
6.基因突变:BRCA增加乳腺癌发病风险。
注:1990年,研究者发现了一种直接与遗传性乳腺癌有关的基因,命名为乳腺癌1号基因,英文简称BRCA1。1994年,又发现另外一种与乳腺癌有关的基因,称为BRCA2。
7.肥胖:一项纳入了12项观察性研究的系统评价和Meta分析结果显示,在队列研究中脂肪含量最高的人群患乳腺癌风险为脂肪含量最低的人群的1.44倍。在2018年发布的癌症预防报告(第3版)中汇总了肥胖与绝经前或绝经后女性乳腺癌发病风险的相关证据,大量流行病学证据和剂量-反应关系分析支持同样的结论,即肥胖会增加绝经后女性乳腺癌的发病风险。
8.生活方式因素:
1.饮酒:饮酒人群的乳腺癌发病风险增高,有饮酒史人群患乳腺癌的风险为无饮酒史人群的1.16倍;
2.吸烟:吸烟人群乳腺癌的发病风险增高。有吸烟史人群的乳腺癌发病率为非吸烟人群的1.13倍。
9.暴露于治疗性电离辐射:
暴露于治疗性电离辐射的女性患乳腺癌的风险增高。行多次胸部透视检查的女性肺结核患者患乳腺癌的风险增加。年轻时胸部暴露于电离辐射如接受过放射治疗的霍奇金淋巴瘤的女性,其患乳腺癌的风险增加,且女童肿瘤患者接受高剂量放疗后乳腺癌标化发病率比为24.20(95% CI:20.70~28.30)。另一项研究显示,乳腺癌的发病风险随胸部放射剂量呈线性增加,与乳腺癌发病风险相关的电离辐射因素包括照射时的年龄、照射持续时间和辐射剂量等。45岁后乳腺X线检查提示乳腺实质(或乳房密度)类型为不均匀致密性或致密性为患乳腺癌高风险人群。
二:乳腺癌目前研究已明确的保护因素:
1. 母乳喂养:现有研究表明,母乳喂养可以降低乳腺癌的发病风险。一项评估母乳喂养对孕产妇健康结果影响的系统评价提示,12个月母乳喂养可使患乳腺癌的风险降低26%,有力的说明了母乳喂养是乳腺癌的保护因素。且可看出与从不母乳喂养者相比,曾经母乳喂养者乳腺癌的患病风险下降22%。
2. 体育锻炼:流行病学研究证据显示,适当的体育锻炼可以降低女性乳腺癌的发病风险,例如慢跑、做瑜伽等。
三.X线摄影诊断评估分类:
1.乳腺癌的组织学分型包括:
①非浸润性癌:
导管原位癌:乳腺导管内原位癌(ductal carcinoma in situ, DCIS)外科治疗包括:肿瘤单纯切除术和全乳房切除。全乳房切除术是DCIS根治性治疗手段,大约98%~99%患者接受这一手术治疗。全乳房切除术后复发几乎全是浸润性癌,表现为局部复发或局部没有复发而远处转移。全乳房切除术是最有效的DCIS治疗手段,但是对一个一生都不会进展成浸润性癌的DCIS患者,实施这种手术有过度治疗之嫌。浸润性乳腺癌保乳术的成功,使人们进而转向探讨保乳术治疗DCIS的可能。
小叶原位癌:小叶原位癌(lobular carcinoma in situ)来自小叶的终末导管及腺泡,主要累及小叶,癌细胞局限于管泡内,未穿破其基底膜,小叶结构存在。
②浸润性癌:
浸润性癌非特殊型;浸润性小叶癌;
小管癌:乳腺小管癌是一种预后极好、由高分化小管结构所组成的特殊类型的乳腺癌。
黏液癌:乳腺粘液腺癌也称粘液样癌或胶样癌,是原发于乳腺的一种很少见的特殊类型的乳腺癌,通常肿瘤生长缓慢,转移较少见,预后比其他类型乳腺癌为好,占所有乳腺癌发病率的1.4% -5.2%。发病年龄多在33岁-91岁,多数西方国家的研究报道乳腺粘液腺癌的发病年龄在50~59岁,以高龄和闭经后患者高发。而来自日本国的报道则认为,乳腺粘液腺癌以闭经前和年轻患者多发。因此世界不同地区之间在发病年龄上可能存在差异。
2.根据美国癌症联合会(American Joint Committee on Cancer, AJCC)TNM分期系统(第8版),乳腺癌分为0期、Ⅰ期、Ⅱ期、Ⅲ期和Ⅳ期
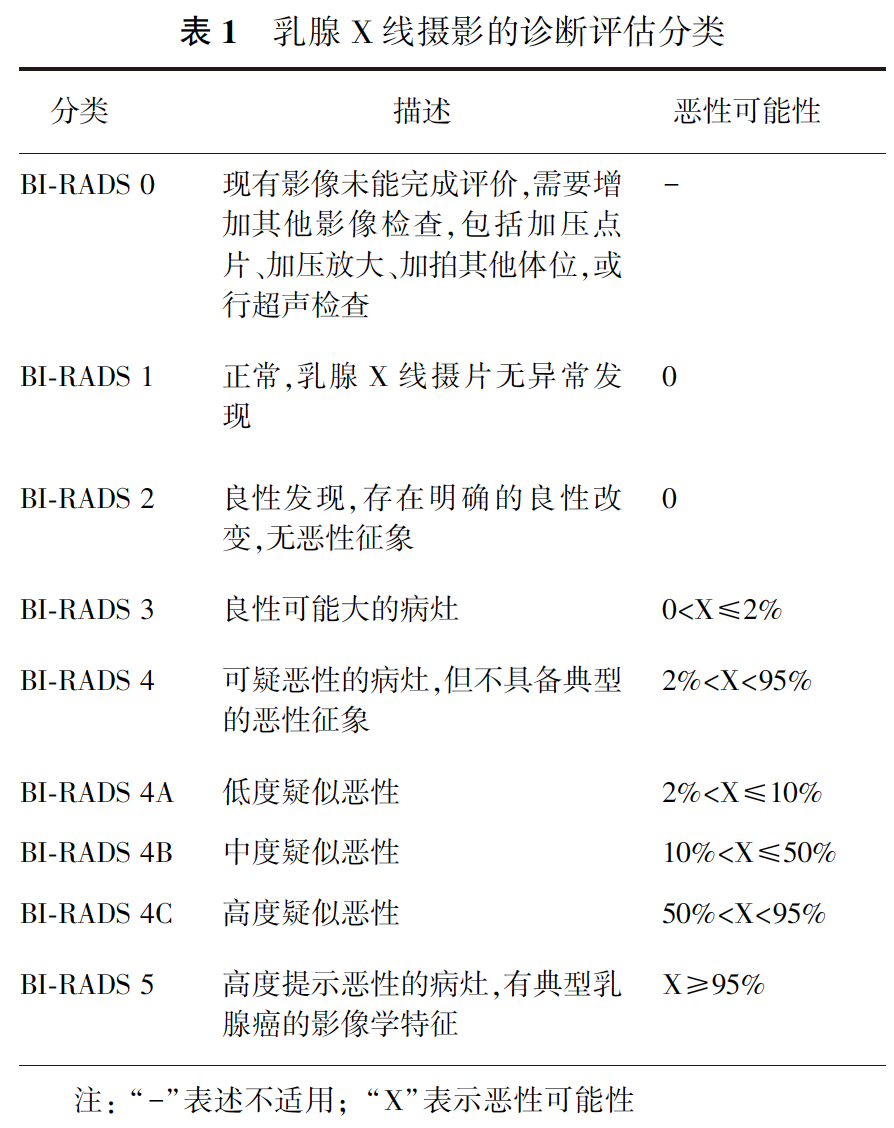
乳腺X线摄影的诊断评估分类应符合表1的规定。
3.筛查结果按下列规定进行管理:
①. BI-RADS 1和BI-RADS 2:无需处理;
②. BI-RADS 3:乳腺X线摄影评估为BI-RADS 3,最好在第一次检查后6个月时对病灶侧乳腺再进行乳腺X线摄影复查,第12个月和24个月时对双侧乳腺进行乳腺X线摄影复查。如果病灶位置保持稳定,则可继续复查;2~3年随访无变化者可以降为BI-RADS 2,病灶会因生活习惯和情绪变大或变小,所以如果复查过程中病灶消失或缩小,可直接评估为BI-RADS 2或 BI-RADS 1。若复查过程中病灶有可疑发现,应考虑活检。乳腺超声评估为BI-RADS 3,复查最佳时间段为3~6个月行乳腺超声检查,2年随访无变化者可降为BI-RADS 2;
较为严重:
③. BI-RADS 4A:应进一步影像检查,必要时活检;
④. BI-RADS 4B:应进一步影像检查,宜进行活检;
⑤. BI-RADS 4C和BI-RADS 5:应进行活检。
尚医云·小济医生-人工智能乳腺癌早筛机器人
四.乳腺影像诊断相关定义:
(一)乳腺实质(或乳房密度)类型
1.乳腺实质类型分为:
(1). 脂肪型;
(2). 散在纤维腺体型;
(3). 不均匀致密型(可能掩盖小肿块);
(4). 致密型(降低乳腺癌检出的敏感性)。
(二)、病灶变化:病灶描述为
(1). 部位:注明左侧和(或)右侧;
(2). 象限及钟面标明:外上象限、内上象限、外下象限、内下象限、乳晕下、中央区、腋尾;
(3). 深度:自乳头向后,用前、中、后1/3描述深度;
(4). 注明病灶距乳头的距离。
(三)异常征象:异常征象有肿块、钙化、结构扭曲、不对称、乳腺内淋巴结、皮肤病变、单侧扩张的导管及伴随征象。
1. 肿块:肿块表现在两个不同投照位置均可见的占位性病变,按下列描述内容进行。
(1)形状:圆形、卵圆形、不规则形;
(2)边缘:
①清晰:至少75%的肿块边界与周围正常组织分界清晰、锐利,其余部分边缘可被周围腺体遮盖,但无浸润或毛刺征象。若任何边缘有浸润或毛刺的肿块,应判断为下述④或⑤;
② 遮蔽状:肿块被重叠或邻近的正常组织遮盖住,无法对其作进一步判断,或者判断失误,阅片医师认为这个肿块的边界是清晰的,只是被周围腺体遮盖;
③ 微小分叶:边缘呈小波浪状改变;
④ 浸润:病灶本身向周围浸润而引起的边界不规则,而不是由于周围腺体遮盖所致;
⑤ 毛刺:从肿块边缘发出的放射状线影。
(3)密度:与肿块周围相同体积的乳腺组织相比较,可分为高密度、等密度、低密度(不含脂肪)和含脂肪密度。
2. 钙化:钙化的形态和分布描述为:
(1)形态:
① 典型良性钙化:包括:皮肤钙化、血管钙化、粗大或爆米花样钙化、大杆状钙化、圆形钙化、环形钙化、营养不良性钙化、钙乳的钙化和缝线钙化等;
② 可疑形态钙化:包括不定形或模糊不清的钙化、粗大不均质钙化、细小多形性钙化(直径常<0.5 mm)、细线样或细线分支样钙化;后者常提示被乳腺癌侵犯的导管腔内钙化。
(2)典型良性钙化不用描述其分布,可疑钙化的分布描述为:
① 弥漫分布;
② 区域性分布:较大范围内分布的钙化,不符合导管分布,常>2 cm2,这种钙化分布的性质应结合形态综合考虑;
③ 簇群分布:指至少有5枚钙化占据较少的范围内(<1 cm2),更多钙化成堆聚集,范围在2 cm2;
④ 线样分布:钙化排列成线状,位于导管内;
⑤ 段样分布:源于一个导管及其分支。
3. 结构扭曲:正常结构被扭曲但无明确的肿块可见,包括从一点发出的放射状影和局灶性收缩,或者在实质的边缘扭曲。
4. 不对称:不对称征象按下列内容进行描述:
(1)结构不对称:仅在一个投照位置上可见的纤维腺体组织,绝大部分是正常腺体组织的重叠所致;
(2)整体不对称:较大范围腺体的不对称,至少达1个象限,不伴有其他征象,多为正常变异。但当与临床触及的异常相吻合时,则可能有意义;
(3)局灶性不对称:两个投照位置均显示且表现相仿,但缺少真性肿块特有的外凸边缘改变,常为内凹,较球形不对称范围小。它可能代表的是1个正常的腺体岛(尤其当其中含有脂肪时)。但在缺乏特征性的良性征象时,往往需要对其做进一步检查,由此可能会显示1个真性肿块或明显的结构扭曲改变;
(4)进展性不对称:新发、增大的或比以前更明显的局灶性不对称。
5. 乳腺内淋巴结:乳腺内淋巴结典型表现为肾形,肉眼可见淋巴结门脂肪所致的透亮切迹,常<1 cm。当淋巴结较大,但其大部分为脂肪替代时,仍为良性改变。可以是多个,也可能是1枚淋巴结由于明显的脂肪替代看上去像多个圆形结节影。对于乳腺外上部的特征性改变可以作出正确诊断。偶尔也可出现在其他区域,多与静脉伴行。
6. 皮肤病变:皮肤病变投照在乳腺组织内,尤其是两个投照体位都有显示的时候,应在评估报告中提及。摄片的技术员应在皮肤病变处放一个不透X线的标志。
7. 单侧扩张的导管:管状或分支样结构可能代表扩张或增粗的导管。
8. 相关伴随征象。
文章来源于:中华肿瘤杂志,作者中华肿瘤杂志

 让我们聊聊关于乳腺癌那点事
让我们聊聊关于乳腺癌那点事